2. क्या हमारे आस-पास के पदार्थ शुद्ध है | शुद्ध पदार्थ Science class 9
2. क्या हमारे आस-पास के पदार्थ शुद्ध है | शुद्ध पदार्थ Science class 9
शुद्ध पदार्थ
2. क्या हमारे आस-पास के पदार्थ शुद्ध हैं ?
(विज्ञान-IX)
परिचय:
पिछले अध्याय में हम पढ़ चुके है कि "वह वस्तु जो स्थान घेरता हो और जिसका द्रव्यमान हो वह पदार्थ कहलाता है |"
शुद्ध पदार्थ: वह पदार्थ जिसमे मौजूद सभी कण समान रासायनिक प्रकृति के हो तो वह वैज्ञानिक दृष्टि से शुद्ध पदार्थ कहलाता है | अर्थात शुद्ध पदार्थ एक ही प्रकार के कणों से मिलकर बना है |
तत्व: तत्व पदार्थ का वह मूल (विशुद्ध) रूप है जिसे रासायनिक प्रक्रिया दवारा अन्य सरल पदार्थों में विभाजित नहीं किया जा सकता | जैसे -लोहा, सोना, चाँदी, कार्बन एवं ऑक्सीजन आदि |
सभी धातुएँ, अधातुयें और उपधातुयें तत्व की श्रेणी में आती है |
धातुओं के गुणधर्म :
(1) ये चमकीली होती है |
(2) ये ताप और विद्युत की सुचालक होती है |
(3) धातुएँ अघातवर्ध्य और तन्य होती है |
(4) ये ध्वानिक (प्रतिध्वनिपूर्ण ) होती है |
अधातुओं के गुणधर्म :
(1) ये चमकीली नहीं होती है |
(2) ये ताप और विद्युत की कुचालक होती है |
(3) अधातुयें अघातवर्ध्य और तन्य नहीं होती है |
(4) ये ध्वानिक (प्रतिध्वनिपूर्ण ) नहीं होती है |
उपधातु: कुछ तत्व धातुओं और अधातुओं के बीच के या दोनों के गुणधर्म प्रदर्शित करते है ऐसे तत्वों को उपधातु कहा जाता है है | जैसे - बोरान, सिलिकोन और जर्मेनियम इत्यादि |
यौगिक : दो या दो से अधिक तत्वों के मेल से एक निश्चित अनुपात में रासायनिक प्रक्रिया द्वारा बने पदार्थ को यौगिक कहते है | जैसे - जल, नमक, चीनी, अल्कोहल एवं कार्बन-डाइऑक्साइड आदि यौगिक है |
यौगिक का नाम मिलकर बने तत्वों का नाम
1. जल दो भाग हाइड्रोजन और एक भाग ऑक्सीजन
2. नमक एक भाग सोडियम और एक भाग क्लोरीन
3. कार्बन-डाइऑक्साइड एक भाग कार्बन और दो भाग ऑक्सीजन
नोट: उपरोक्त सभी यौगिक एक निश्चित अनुपात में ही बनते है | इन पदार्थों को बिना रासायनिक प्रक्रिया के अलग नहीं किया जा सकता है | इनमें उपस्थित सभी संघटक बने यौगिक से पूरी तरह भिन्न है |
मिश्रण: ऐसे पदार्थ जो एक या एक से अधिक तत्वों या यौगिक से मिलकर बना होता है मिश्रण कहलाता है | जैसे - जल में चीनी, रक्त, वायु और बालू नमक का मिश्रण आदि |
यौगिक तथा मिश्रण में अंतर :
| मिश्रण | यौगिक |
|
1. तत्व या यौगिक मिलकर मिश्रण का निर्माण करते हैं | 2. यह नया पदार्थ नहीं होता है | 3. इसे भौतिक विधियों से अलग किया जा सकता है | 4. इसमें उपस्थित संघटक अपने अपने गुणधर्म को प्रदर्शित करते है | 5. इसके संघटकों का नियत अनुपात नहीं होता है | |
1. तत्व क्रिया करके नए यौगिक का निर्माण करते हैं | 2. यौगिक नया पदार्थ होता है | 3. इसे सिर्फ रासायनिक विधियों द्वारा ही अलग किया जा सकता है | 4. इसमें उपस्थित संघटक पूरी तरह से भिन्न होते है | 5. इनके संघटकों का नियत अनुपात होता है |
|
तत्व और यौगिक में अंतर :
| तत्व | यौगिक |
|
1. इनमें सिर्फ एक ही प्रकार के परमाणु पाए जाते है | 2. इन्हें नहीं तो भौतिक और नहीं रासायनिक विधियों से ही अलग किया जा सकता है | 3. ये पदार्थों के मूल रूप होते है | |
1. इनमें दो या दो से अधिक प्रकार के परमाणु पाए जाते है | 2. इन्हें सिर्फ रासायनिक विधियों के द्वारा अलग किया जा सकता है | 3. ये तत्वों से बने नए पदार्थ होते है | |

मिश्रण और विलयन के भेद
2. क्या हमारे आस-पास के पदार्थ शुद्ध है ?
(विज्ञान-IX)
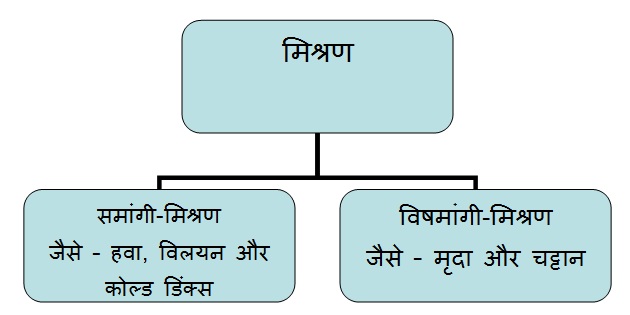
मिश्रण के प्रकार :
मिश्रण दो प्रकार के होते है |
(I) समांगी मिश्रण : वह मिश्रण जिसकी बनावट समान हो तथा इसके कणों को अलग अलग नहीं पहचाना जा सके समांगी मिश्रण कहते है | जैसे : नमक और जल का घोल |
(II) विषमांगी मिश्रण : वह मिश्रण जिसके अंश भौतिक रूप से अलग होते है और इसके कणों को अलग-अलग पहचाना जा सकता है, विषमांगी मिश्रण कहलाता है | जैसे : लोहे के बुरादे और बालू का मिश्रण |
मिश्रण के गुणधर्म:
- मिश्रण के संघटकों को असानी से अलग किया जा सकता है |
- प्रत्येक संघटक का अपना वास्तविक गुणधर्म होता है |
- संघटकों का अनुपात अलग-अलग होता है |
विलयन
विलयन : दो या दो से अधिक पदार्थों के समांगी मिश्रण को विलयन कहते है |
जैसे : निम्बू जल, सोडा जल आदि |
विलयन पदार्थ के तीनो अवस्थाओं में पाया जाता है |
(1) ठोस विलयन : मिश्र धातु |
(2) तरल विलयन : निम्बू-पानी |
(3) गैसीय विलयन : वायु |
विलयन के कण समान रूप से वितरित रहते है, अर्थात इसके कणों को अलग-अलग पहचाना नहीं जा सकता है | जैसे - निम्बू-चीनी पानी में एक ही स्वाद होता है , ऐसा नहीं है कि चखने पर निम्बू का स्वाद अलग प्राप्त हो और चीनी का अलग प्राप्त हो |
विलयन के गुण :
(I) यह एक समांगी मिश्रण है |
(ii) विलयन के कण समान रूप से वितरित रहते है जिन्हें आँखों से देखा नहीं जा सकता है |
(III) विलयन में प्रकाश का मार्ग दिखाई नहीं देता है |
(IV) यह स्थाई होता है |
(V) छानने की विधि से इसके विलेय कणों को पृथक नहीं किया जा सकता है |
विलयन = विलायक + विलेय

विलायक : विलयन का वह घटक जो विलयन में सबसे अधिक मात्रा में होता है और यह दुसरे घटकों को को विलयन में मिलाता है, विलायक कहलाता है | जैसे : जल, अल्कोहल, तारपीन तेल आदि विलायक होते है |
विलेय : विलयन का वह घटक जो विलयन में सबसे कम मात्रा में रहता है और विलायक में घुला रहता है | जैसे : चीनी, नमक, सोडा, पोटेशियम परमैगनेट और आयोडीन आदि |
प्रश्न: वायु के मिश्रण में विलायक और विलेय का नाम बताइए ?
सांद्रता : किसी मिश्रण में इकाई आयतन में उपस्थित किसी पदार्थ की विशेष मात्रा होती है |
विलयन की सांद्रता : रसायन विज्ञान में किसी विलयन की सांद्रता उस विलयन के इकाई आयतन में उपस्थित पदार्थ की मात्रा के रूप में परिभाषित किया गया है। अर्थात,
"किसी विलयन के इकाई आयतन में विलेय पदार्थ की उपस्थित मात्रा को विलयन की सांद्रता कहते है |"
(1) संतृप्त विलयन: वह विलयन जिसमें दिए गए निश्चित ताप पर विलेय पदार्थ जब और अधिक नहीं घुलता तो ऐसे विलयन को संतृप्त विलयन कहते है |
(2) असंतृप्त विलयन: यदि एक विलयन में विलेय पदार्थ की मात्रा संतृप्तता (घुलने की क्षमता ) से कम हो तो ऐसे विलयन को असंतृप्त विलयन कहते है |
(3) अतिसंतृप्त विलयन : यदि किसी विलयन में विलेय पदार्थ की मात्रा (सांद्रता) संतृप्त स्तर से अधिक हो तो इसे अतिसंतृप्त विलयन कहते है |
घुलनशीलता : विलेय पदार्थ की वह मात्रा जो जो दिए गए ताप पर संतृप्त विलयन में उपस्थित है वह विलेय पदार्थ की घुलनशीलता कहलाता है |
कोलाइडल विलयन और टिंडल प्रभाव
2. क्या हमारे आस-पास के पदार्थ शुद्ध है ?
(विज्ञान-IX)
निलंबन : वह विषमांगी घोल जो ठोस द्रव में परिक्षेपित हो जाता है, निलंबन कहलाता है |
निलंबन एक विषमांगी मिश्रण है, जिसमें विलेय पदार्थ के कण घुलते नहीं है बल्कि माध्यम के समष्टि में निलंबित रहते है | ये निलंबित कण आँखों से देखे जा सकते है |
निलम्बन के गुणधर्म :
(1) यह एक विषमांगी मिश्रण है |
(2) ये कण आँखों से देखे जा सकते है |
(3) इनके निलंबित कण प्रकाश के किरण को फैला देते है |
(4) ये अस्थाई होते है |
(5) इन्हें छानने की विधि से अलग किया जा सकता है |
कोलाइडल विलयन : यह एक विषमांगी मिश्रण है, जिसके कण अति सूक्ष्म होने की वजह से दिखाई तो नहीं देते परन्तु कोलाइडल के कण विलयन में समान रूप से फैले रहते है और ये प्रकाश के किरण को असानी से फैला देते है | ऐसा विलयन कोलाइडल विलयन कहलाता है |
जैसे - दूध, धुआं, कोहरा, आदि |
कोलाइडल विलयन के गुणधर्म :
(1) यह एक विषमांगी मिश्रण होता है |
(2) इनका आकार छोटा होने के कारण इन्हें आँखों से देखा नहीं जा सकता है |
(3) ये प्रकाश के मार्ग को दृश्य बनाते है |
(4) छानने की विधि से इसके कणों को पृथक नहीं किया जा सकता है |
(5) ये टिंडल प्रभाव दिखाते है |
कोलाइडल विलयन के संघटक :
परिक्षिप्त प्रावस्था (dispersed Phase): विलेय पदार्थ की तरह का घटक या परिक्षिप्त कण जो की कोलाइडल के रूप में रहता है उसे परिक्षिप्त प्रावस्था कहते है | अर्थात विलेय कणों को परिक्षिप्त प्रावस्था कहते है |
परिक्षेपण माध्यम (Dispersing Medium): वह घटक जिसमे परिक्षिप्त प्रावस्था निलंबित रहता है, परिक्षेपण माध्यम कहते है | अर्थात विलायक जिसमें ये पूरी तरह से वितरित रहते है, उसे परिक्षेपण माध्यम कहते है |
टिंडल प्रभाव (Tyndall Effect):
कोलाइडल के छोटे-छोटे कण प्रकाश के किरण को फैला देते है इस प्रकार प्रकाश के किरण का फैलाना टिंडल प्रभाव (Tyndall Effect) कहते है |
नोट: टिंडल प्रभाव की खोज टिनडल नामक वैज्ञानिक ने की थी |
टिंडल प्रभाव दर्शाने वाले कोलाइड्स के समान्य उदहारण :
दूध, फेस क्रीम, कोहरा, बादल, कुहासा, धुआं, शेविंग क्रीम, मिल्क ऑफ़ मैग्नीशिया, कीचड़, जेली, पनीर, मक्खन इत्यादि |

आप ने घरों की छतों या खिड़कियों से भी टिंडल प्रभाव को देखा होगा |
जब प्रकाश का पुंज इन छिद्रों से होकर गुजरता है तो वायु में उपस्थित कोलाइड्स के कण दृश्य हो जाते है और स्पष्ट देखे जाते है | ऐसा जंगलों में भी देखा जाता है जब घने पेड़ की डालियों के बीच से प्रकाश की किरण गुजरती है तो वायु के कण दृश्य हो जाते है |

मिश्रण के घटकों का पृथक्करण
मिश्रण के घटकों का पृथक्करण
(The Seperation of components of Mixture):
मिश्रण के घटकों को पृथक करने के लिए विभिन्न प्रकार की विधियां प्रयोग में लाई जाती है |
विषमांगी मिश्रण को साधारण भौतिक क्रिया द्वारा पृथक किया जा सकता है, जैसे हाथ से चुनकर या छन्नी से छानकर आदि | परन्तु कभी-कभी इन घटकों को अलग करने के लिए विशेष तकनीकों का भी प्रयोग किया जाता है |
मिश्रण के घटकों को पृथक करने की निम्न विधियाँ है :
(1) वाष्पीकरण विधि
(2) अपकेन्द्रण विधि
(3) पृथक्करण विधि
(4) उर्ध्वपातन विधि
(5) क्रोमैटोग्राफी विधि
(6) आसवन विधि या प्रभाजी असवान विधि
(7) क्रिस्टलीकरण विधि
1. वाष्पीकरण विधि : इस विधि में द्रवीय पदार्थ को गर्म करके वाष्पीकृत कर दिया जाता है और मिश्रण के बाकी कण शेष रह जाते है |
अनुप्रयोग :
(i) समुद्री जल से नमक प्राप्त करने में |
(ii) जल से काले रंग की स्याही को अलग करने में |
2. अपकेन्द्रण विधि : यह वह विधि है जिसमे एक अपकेन्द्रिय यन्त्र का प्रयोग किया जाता है जोकि एक प्रकार की मथनी या मिक्सी होती है जिसे मिश्रण में इसे तेजी से घुमाया जाता है तो भारी कण निचे बैठ जाते है और हलके कण ऊपर ही रह जाते है |
अनुप्रयोग :
(i) जाँच प्रयोगशाला में रक्त और मूत्र के जाँच में |
(ii) डेयरी तथा क्रीम से मक्खन निकालने की प्रक्रिया में |
(iii) कपडे धोने की मशीन में |
3. पृथक्करण विधि : इस विधि के द्वारा दो अघुलनशील द्रवों के मिश्रण को अलग किया जाता है | पृथक्करण के सिद्धांत के अनुसार, आपस में नहीं मिलाने वाले द्रव अपने घनत्व के अनुसार विभिन्न परतों में पृथक हो जाते है |
अनुप्रयोग: '
(i) तेल तथा जल के अघुलनशील मिश्रण को पृथक करने में |
(ii) धातुशोधन के दौरान लोहे को पृथक करने में |
4. उर्ध्वपातन विधि : इस विधि के द्वारा उर्ध्वापतित होने वाले पदार्थों को उर्ध्वापतित ना होने वाले अशुद्धियों से अलग करने के लिए उपयोग किया जाता है | कुछ उर्ध्वापतित होने वाले पदार्थ जैसे अमोनिया क्लोराइड, कपूर, नेफ्थालिन और एन्थ्रासीन इसके उदहारण है |
अनुप्रयोग :
(i) अमोनियम क्लोराइड और नमक के मिश्रण को अलग करने में |
(ii) कपूर और लोहे के बुरादे को अलग करने में |
5. क्रोमाटोग्राफी विधि : इस विधि का प्रयोग उन विलेय पदार्थों को पृथक करने में किया जाता है जो एक ही प्रकार के विलायक में घुले रहते है | मिश्रण से घटकों के पृथक करने की उस विधि को क्रोमाटोग्राफी कहते है |
अनुप्रयोग :
(i) डाई में रंगों को अलग करने में |
(ii) प्राकृतिक रंगों से पिगमेंट को पृथक करने में |
(iii) रक्त से नशीले पदार्थों को अलग करने में |
6. प्रभाजी आसवन विधि :
आसवन विधि का उपयोग वैसे मिश्रण को पृथक करने में किया जाता है जो विघटित हुए बिना उबलते हैं तथा जिनके घटकों के क्वथनांकों के मध्य अधिक अन्तराल होता है |
दो या दो से अधिक घुलनशील द्रवों जिनके क्वथनांक का अंतर 25 K से कम होता है, के मिश्रण को अलग करने में इस विधि का प्रयोग किया जाता है |
प्रभाजी स्तंभ : प्रभाजी जी स्तंभ एक नली होती है जो कि शीशे के गुटकों से भरी होती है | ये गुटके वाष्प को ठंडा और संघनित होने के लिए सतह प्रदान करते हैं |
वायु के घटकों का पृथक्करण : जब हमें वायु से ऑक्सीजन गैस को प्राप्त करना चाहते हैं तो हमें वायु में उपस्थित दूसरी गैसों जैसे कार्बन डाइऑक्साइड एवं नाइट्रोजन को पृथक करना होता है | द्रव वायु प्राप्त करने के लिए पहले वायु पर दबाव बढाया जाता है और फिर ताप को घटाकर उसे ठंडा कर संपीडित किया जाता है और इस द्रवित गैस को प्रभाजी आसवन स्तंभ में धीरे=धीरे गर्म किया जाता है, जहाँ सभी गैसे विभिन्न ऊँचाइयों पर अपने क्वथनांक के अनुसार पृथक हो जाती है |
- इस विधि में जब वायु को ठंडा किया जाता है तो कार्बन डाइऑक्साइड जो वायु का एक प्रमुख घटक है शुष्क बर्फ़ के रूप में निर्गत होता है |
अनुप्रयोग :
(i) वायु से विभिन्न गैसों का पृथक्करण |
(ii) पेट्रोलियम उत्पादों को उनके विभिन्न घटकों का पृथक्करण |
7. क्रिस्टलीकरण विधि : क्रिस्टलीकरण वह विधि है जिसके द्वारा क्रिस्टल के रूप में शुद्ध ठोस को विलयन से पृथक किया जाता है |
इस विधि का प्रयोग ठोस पदर्थों को शुद्ध करने में किया जाता है | उदहारण : समुद्री जल से प्राप्त नमक की अशुद्धियों को अलग करने में |
अनुप्रयोग :
(i) समुद्री जल से प्राप्त नमक को शुद्ध करने में |
(ii) अशुद्ध नमूने से फिटकिरी को पृथक करने में |
- क्रिस्टलीकरण विधि साधारण वाष्पीकरण विधि से उत्तम होती है | जिसके निम्न कारण हैं |
(1) कुछ ठोस विघटित हो जाते हैं या कुछ चीनी के सामान गर्म करने पर झुलस जाते हैं |
(2) छानने के पश्चात् भी अशुद्ध विलेय पदार्थ को विलायक में घोलने पर विलयन में कुछ अशुद्धियाँ रह सकती हैं | वाष्पीकरण होने पर ये अशुद्धियाँ ठोस को दूषित कर सकती हैं |
भौतिक गुण :
ऐसे गुण जिनका हम अवलोकन एवं वर्णन कर सकते हैं, भौतिक गुण कहलाते है |
जैसे - रंग, कठोरता, दृढ़ता, बहाव, घनत्व, द्रवनांक तथा क्वथनांक आदि |
भौतिक परिवर्तन और रासायनिक परिवर्तन में अंतर:


भौतिक परिवर्तनों का उदाहरण :
पेड़ों को काटना, बर्फ़ का पिघलना, जल का साधारण नमक में घुलना, फलों से सलाद बनाना आदि |
रासायनिक परिवर्तनों का उदाहरण :
भोजन का पचना, भोजन का पकना, लोहे पर जंग लगना, सब्जियां काटने से चाकू का रंग बदलना लकड़ी एवं कागज का जलना आदि |
Share this Notes to your friends:
Science Chapter List
1. हमारे आस-पास के पदार्थ
2. क्या हमारे आस-पास के पदार्थ शुद्ध है
3. परमाणु एवं अणु
4. परमाणु की संरचना
5. जीवन की मौलिक इकाई
6. ऊत्तक
7. जीवों में विविधता
8. गति
9. बल और गति का नियम
10. गुरुत्वाकर्षण
11. कार्य और उर्जा
12. ध्वनि
13. हम बीमार क्यों होते है
14. प्राकृतिक संसाधन
15. खाद्ध्य संसाधनों में सुधार
Select Class for NCERT Books Solutions
NCERT Solutions
NCERT Solutions for class 6th
NCERT Solutions for class 7th
NCERT Solutions for class 8th
NCERT Solutions for class 9th
NCERT Solutions for class 10th
NCERT Solutions for class 11th
NCERT Solutions for class 12th
sponder's Ads